近期,咨询第一类医疗器械委托生产的企业较多,特整理了该篇内容,供大家参考。第一类医疗器械在中国上市前需要取得医疗器械产品备案证和医疗器械生产备案证。
第一类医疗器械产品备案
医疗器械备案是指医疗器械备案人(以下简称备案人)依照法定程序和要求向药品监督管理部门提交备案资料,药品监督管理部门对提交的备案资料存档备查的活动。境内第一类医疗器械备案人向所在地区的市级药品监督管理部门提交备案资料,进口第一类医疗器械备案人是向国家药品监督管理局提交备案资料。以下是第一类医疗器械备案流程:
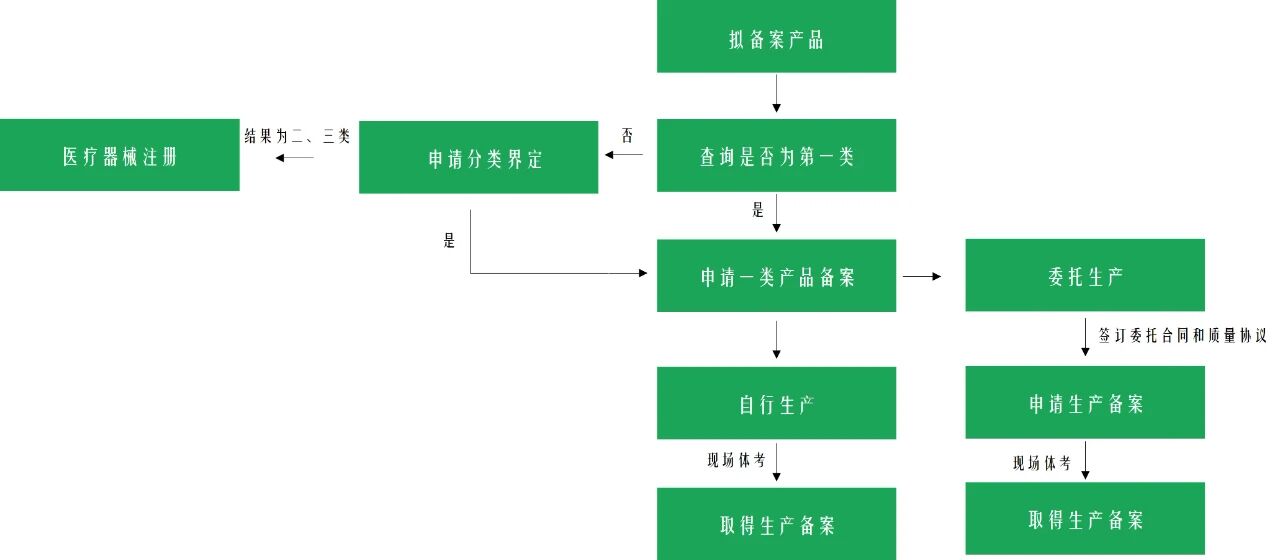
在进行第一类医疗器械备案时,我们首先需要判定产品的管理类别,结合产品实际情况,根据《第一类医疗器械产品目录》、《体外诊断试剂分类子目录》等规定中产品描述、预期用途的品名举例进行判定。如果超出目录内容,可以根据相关工作程序申请分类界定,明确产品管理类别是否为第一类医疗器械,再提交符合法规要求的备案资料,获取备案号。
备案资料要求
(一)第一类医疗器械备案表
2022年,国家局发布了《国家药监局关于第一类医疗器械备案有关事项的公告(2022年第62号)》、《<关于第一类医疗器械备案有关事项的公告>修订说明》,简化了备案资料提交的项目,一是删除了备案资料中的“风险分析报告”。二是删除了临床评价资料的要求。
第一类医疗器械生产备案
根据新版《医疗器械监督管理条例》第三十四条,医疗器械注册人、备案人可以自行生产医疗器械,也可以委托符合本条例规定、具备相应条件的企业生产医疗器械。
备案人委托生产
